Новые пути лечения аллергии
Новое международное исследование выявило в организме человека большое количество В-лимфоцитов, продуцирующих антитела группы Е, так называемые IgE (иммуноглобулин E).
Эти антитела стоят за аллергическими реакциями и распространены у трети населения мира. Они проявляются в высоких уровнях при астме, ангионевротическом отеке и анафилаксии – состояниях, которые тяжело протекают или непосредственно опасны для жизни.
Исследование, опубликованное в журнале Cells, ставит целью углубить понимание того, как протекают эти реакции и как с ними можно бороться, чтобы улучшить качество жизни пациентов.
Иммуноглобулин E
Молекулы иммуноглобулина (Ig) производятся определенным типом иммунной клетки (В-лимфоциты) или позже ее зрелой формой – плазматической клеткой. Эти молекулы сформировались у нас в организме для выявления антигенов или распознавания иных молекул, которые присутствуют на поверхности других тел / бактерий и попадают в наш организм.
Иммуноглобулины помогают иммунной системе устранять или нейтрализовывать эти чужеродные молекулы. Когда такая реакция нейтрализации становится сверхактивной или длится дольше необходимого времени, мы называем это аллергической реакцией.
Иммуноглобулин E – тип иммуноглобулинов, который почти всегда оказывается причастным к зарождению аллергического ответа, то есть к сенсибилизации, а также к поздней фазе этого ответа.
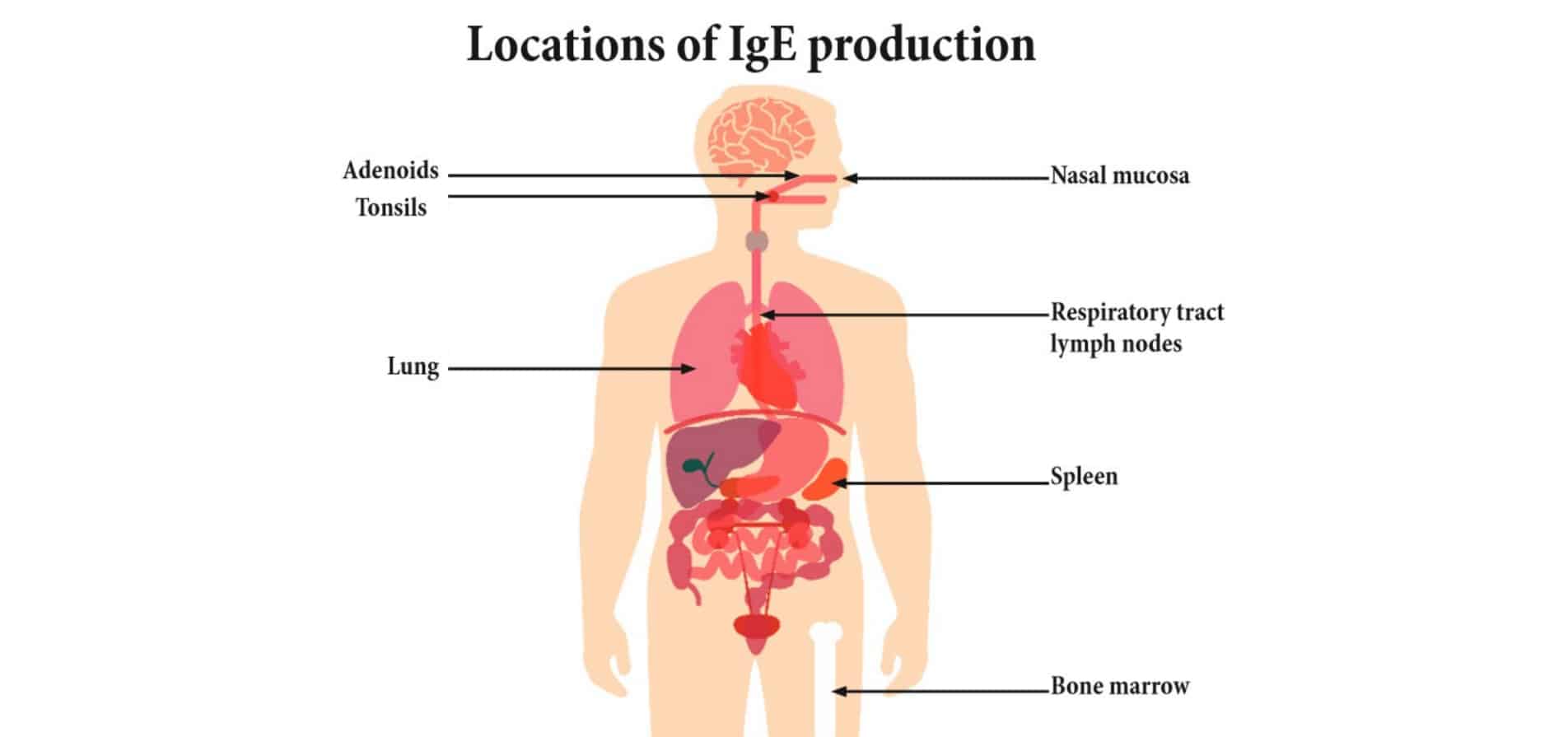
Потенциальные места выработки IgE
Иммуноглобулин E отличается от других антител тем, что присутствует в сыворотке крови в очень низких концентрациях (5×10-5 мг/мл) и имеет очень короткую продолжительность действия. Фактически 50 % молекул IgE разрушаются в течение 2 дней. Для сравнения: у другого класса антител – IgG1 — этот срок составляет 21 день. Низкая концентрация IgE затрудняет анализ этих молекул.
Изучение связи между иммуноглобулином E и лечением аллергии
Гипотетически аллергию можно лечить, удаляя иммуноглобулины E из кровообращения, но проблема заключается в их скором возврате к нормальному или высокому уровню. Иными словами, происходит постоянная, хотя и в небольших количествах, выработка этих молекул. Это подтолкнуло исследователей к определению локализации и уточнения клеток, из которых происходят иммуноглобулины E.
Чтобы понять, как аллергия развивается и как ее можно лечить, для создания модели болезни часто использовались лабораторные мыши. Хотя создание моделей на грызунах было полезным, мыши и люди во многом отличаются, включая индукцию аллергической реакции и ее механизмы.
Кроме того, модель лабораторной аллергии на мышах отличается многогранным воздействием аллергенов, которые индуцируют и модулируют иммунный ответ у человека. Это касается механизмов, благодаря которым концентрация IgE увеличивается при аллергии.
Иммунные клетки, продуцирующие IgE, – это клетки памяти. Они помнят, как выглядят аллергены, в течение многих лет. Поэтому в следующий раз, когда клетки памяти испытывают влияние антигенов (аллергенов), уровень иммуноглобулина E быстро поднимается.
Этот вывод привел к гипотезе о том, что существуют два специфических механизма выработки IgE. Первый – создание постоянного «источника» IgE, который регулярно производит эти молекулы и, возможно, состоит из плазматических клеток. Второй – аллерген-индуцированный всплеск продукции IgE.
Выделение клеток, продуцирующих IgE

Для исследования этих механизмов ученым нужно было выделить В-клетки, продуцирующие иммуноглобулин E, из крови.
Проточная цитометрия – одна широко применяемых для этого методик, которая заключается в наблюдении с помощью лазера за высокоскоростной струей жидкости, где «подвешены» клетки. Они обрабатываются флуоресцентными антителами, которые прижимаются к соответствующим структурам на поверхности В-клеток и IgE-рецепторов, чтобы идентифицировать те по полученному флуоресцентному свечению.
Затем светящиеся клетки подсчитывают. Однако при этой методике выявляется очень много ошибочно положительных клеток, несущих IgE. И только около 0,0019 % выделенных В-клеток являются на самом деле продуцирующими IgE.
Поэтому исследователи предлагают использовать флуоресцентное моноклональное антитело к IgE. Оно будет отделять IgE, связанные только с рецепторами, от тех, которые на самом деле связаны с мембраной, то есть продуцируются самой клеткой.
Предыдущие исследования показали, что плазматическими клетками производится только примерно 0,2 % сывороточного иммуноглобулина E. Подавляющее большинство IgE происходит из других клеток, расположенных в различных периферических участках: от слизистой оболочки носа, которая осуществляет начальный контакт с молекулами аллергена, до легких и миндалин.
IgE также производятся в селезенке и костном мозге. Клетки в периферических местах восстанавливаются с помощью клеточной популяции, циркулирующей в крови.
IgE-опосредованная активация Т-клеток
IgE присоединяется к аллергену, образуя комплекс. Тот связывается с молекулой CD23 на поверхности В-клеток. Это заставляет В-клетки поглощать IgE с аллергеном, а впоследствии – обрабатывать, и представлять Т-клеткам пептид, производный от аллергена. Этот пептид распознается конкретными Т-клетками.
Такой механизм называется IgE-облегченной презентацией аллергена. Он стимулирует активацию и размножение Т-клеток.
Терапия, направленная против иммуноглобулина E

Уровень IgE может быть снижен новыми препаратами, ингибирующими молекулы или клетки, которые их производят.
В первом случае лекарственные средства связываются с определенными специфическими частями домена IgE. Он определяет присоединение молекулы к иммунным клеткам, которые выполняют задачи нейтрализации, уничтожения либо разрушения чужеродных частиц или клеток, переносящих антиген.
Таким образом ограничивается количество активных молекул IgE, способных соединяться с этими иммунными клетками. В свою очередь это уменьшает количество активного воспаления, которое может возникнуть в результате ответа иммунных клеток на аллерген.
Во втором случае В-клетки, продуцирующие IgE, блокируются с помощью связывания препарата с IgE на поверхности клетки. Таким образом В-лимфоцит помечается, становится «видимым» для Т-клеток, которые могут разрушать В-лимфоциты и этим препятствовать чрезмерной продукции IgE.
Статья завершается выводом: механизмы аллергии и синтеза IgE требуют дальнейшего изучения, которое приведет к разработке более эффективных методов лечения аллергии.
Сейчас ученым известны: источники продукции IgE, расположение таких клеток, механизмы, вызывающие повышение уровня IgE, когда организм подвергается воздействию аллергена, и скорость стимуляции рецепторов в ответ на такие изменения. Поэтому работа над созданием новых молекулярных методов лечения аллергии продолжается.

 Стаття рецензована медичним экспертом:
Стаття рецензована медичним экспертом:








