Нові шляхи лікування алергії
Нове міжнародне дослідження виявило в організмі людини велику кількість В-лімфоцитів, які продукують антитіла групи Е, так звані IgE (імуноглобулін E).
Ці антитіла стоять за алергічними реакціями та є поширеними у третини населення світу. Вони виявляються у високих рівнях при астмі, ангіоневротичному набрякові та анафілаксії — станах, які протікають важко чи безпосередньо є небезпечними для життя.
Дослідження, опубліковане в журналі Cells, має на меті допомогти просунути розуміння того, як протікають ці реакції та як з ними можна боротися, щоб поліпшити якість життя пацієнтів.
Імуноглобулін E
Молекули імуноглобуліну (Ig) виробляються певним типом імунної клітини (В-лімфоцитом), або пізніше її зрілою формою — плазматичною клітиною. Ці молекули сформувались у нас в організмі для виявлення антигенів або розпізнавання інших молекул, що присутні на поверхні інших тіл / бактерій та потрапляють до нашого організму.
Імуноглобуліни допомагають імунній системі усунути або нейтралізувати ці чужорідні молекули. Коли така реакція нейтралізації стає надактивною або триває за межами необхідного часу, ми називаємо це алергічною реакцією.
IgE — це тип імуноглобулінів, який майже завжди виявляється причетним до зародження алергічної відповіді, тобто до сенсибілізації, а також до пізньої фази цієї відповіді.
Потенційні місця продукування IgE
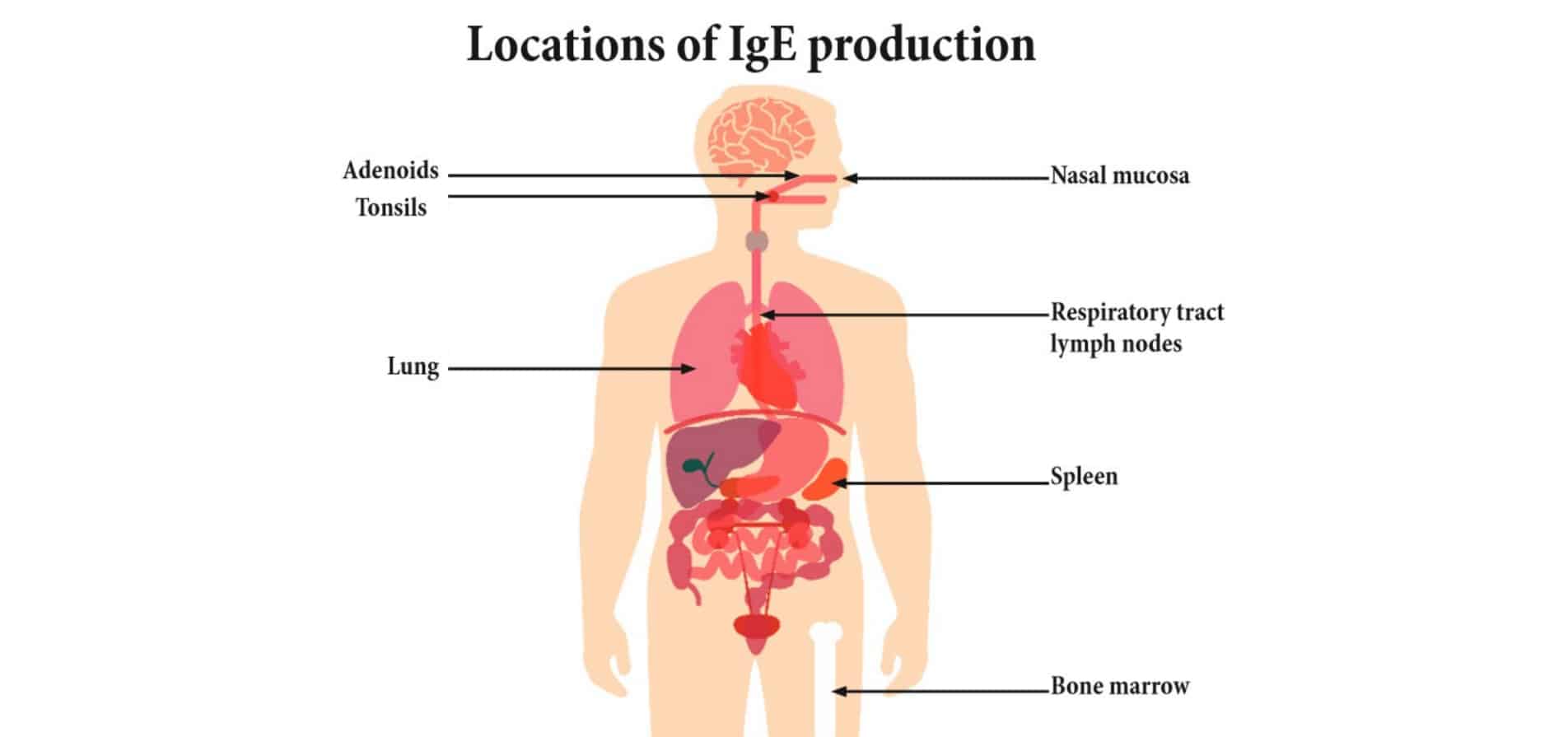
Імуноглобулін E відрізняється від інших антитіл тим, що присутній в сироватці крові у дуже низьких концентраціях (5×10-5 мг/мл) і має дуже коротку тривалість дії. Фактично 50 % молекул IgE руйнуються протягом 2 днів проти 21 дня у IgG1 — іншого класу антитіл. Низька концентрація ускладнює аналіз цих молекул.
Вивчення зв’язку між імуноглобуліном E та лікуванням алергії
Гіпотетично алергію можна лікувати, видаляючи IgE з кровообігу, але проблема полягає в їх швидкому поверненні до нормального або високого рівня. Іншими словами, відбувається постійне, хоч і у невеликих кількостях, вироблення цих молекул. Це підштовхнуло дослідників до визначення локалізації та уточнення клітин, з яких IgE беруть своє походження.
Щоб зрозуміти, як алергія розвивається та як її можна лікувати, для створення моделі хвороби часто використовувались лабораторні миші. Хоча створення моделей на гризунах було корисним, миші та люди багато в чому різняться, включаючи індукцію алергічної реакції і її механізми.
Крім того, модель лабораторної алергії на мишах відрізняється багатогранним впливом алергенів, які індукують та модулюють імунну відповідь у людини. Це стосується механізмів, завдяки яким концентрація IgE збільшується при алергії.
Імунні клітини, що продукують імуноглобулін E, — це клітини пам’яті. Вони пам’ятають, як виглядають алергени протягом багатьох років. Тому наступного разу, коли клітини пам’яті потрапляють під вплив антигенів (алергенів), рівень IgE швидко підіймається.
Цей висновок призвів до гіпотези, що існують два специфічні механізми вироблення IgE. Перший — створення постійного «джерела» IgE, яке регулярно виробляє ці молекули й, можливо, складається з плазматичних клітин. Другий — алерген-індукований сплеск продукції IgE.
Виділення клітин, які продукують імуноглобулін E

Для дослідження цих механізмів вченим потрібно було виділити В-клітини, що продукують IgE, з крові.
Проточна цитометрія — одна з широко застосовуваних для цього методик, яка полягає у спостереженні за допомогою лазера за високошвидкісним струменем рідини, в якій «підвішені» клітини. Вони обробляються флуоресцентними антитілами, які будуть притискатися до відповідних структур на поверхні В-клітин та IgE-рецепторів, щоб ідентифікувати їх за отриманим флуоресцентним сяйвом.
Потім клітини, що світяться, підраховують. Однак при цій методиці визначається дуже багато помилково позитивних клітин, що несуть IgE. І лише близько 0,0019 % виділених В-клітин є насправді такими, що продукують IgE.
А тому дослідники пропонують використовувати флуоресцентне моноклональне антитіло до IgE. Воно буде відділяти IgE, пов’язані лише з рецепторами, від тих, які насправді пов’язані з мембраною, тобто продукуються самою клітиною.
Попередні дослідження показали, що плазматичними клітинами виробляється лише приблизно 0,2 % сироваткового IgE. Переважна більшість походить з інших клітин, розташованих у різних периферичних ділянках: від слизової оболонки носа, яка здійснює початковий контакт з молекулами алергену, до легенів та мигдалин.
IgE також виробляються в селезінці та кістковому мозку. Клітини в периферичних місцях відновлюються за допомогою клітинної популяції, що циркулює в крові.
IgE-опосередкована активація Т-клітин
IgE приєднується до алергену, утворюючи комплекс. Він зв’язується з молекулою CD23 на поверхні В-клітин. Це змушує В-клітини поглинати IgE з алергеном, а згодом — обробляти, та представляти Т-клітинам пептид, похідний від алергену. Цей пептид розпізнається конкретними Т-клітинами.
Такий механізм має назву IgE-полегшеного представлення алергену. Він стимулює активацію та розмноження Т-клітин.
Терапії, спрямовані проти імуноглобуліну E

Рівень IgE може бути знижений новоствореними препаратами, які інгібують або молекули, або клітини, що їх виробляють.
У першому випадку лікарські засоби зв’язуються з певними специфічними частинами домену IgE. Він визначає приєднання молекули до імунних клітин, які виконують завдання нейтралізації, вбивання або руйнування чужорідних частинок або клітин, що переносять антиген.
Таким чином обмежується кількість активних молекул IgE, які можуть з’єднуватися з цими імунними клітинами. В свою чергу це зменшує кількість активного запалення, яке може виникнути в результаті відповіді імунних клітин на алерген.
У другому випадку В-клітини, які продукують IgE, блокуються за допомогою зв’язування препарату з IgE на поверхні клітини. Таким чином В-лімфоцит позначається, стає «видимим» для Т-клітин, які можуть зруйнувати В-лімфоцити й цим перешкодити надмірній продукції IgE.
Стаття завершується висновком, що механізми алергії та синтезу IgE потребують подальшого вивчення, яке призведе до розробки ефективніших методів лікування алергії.
Наразі вченим відомі: джерело продукції IgE, розташування таких клітин, механізми, що викликають підвищення рівня IgE, коли організм піддається впливу алергену, та швидкість стимуляції рецепторів у відповідь на такі зміни. Тож робота над створенням нових молекулярних методів лікування алергії продовжується.

 Стаття рецензована медичним экспертом:
Стаття рецензована медичним экспертом:








